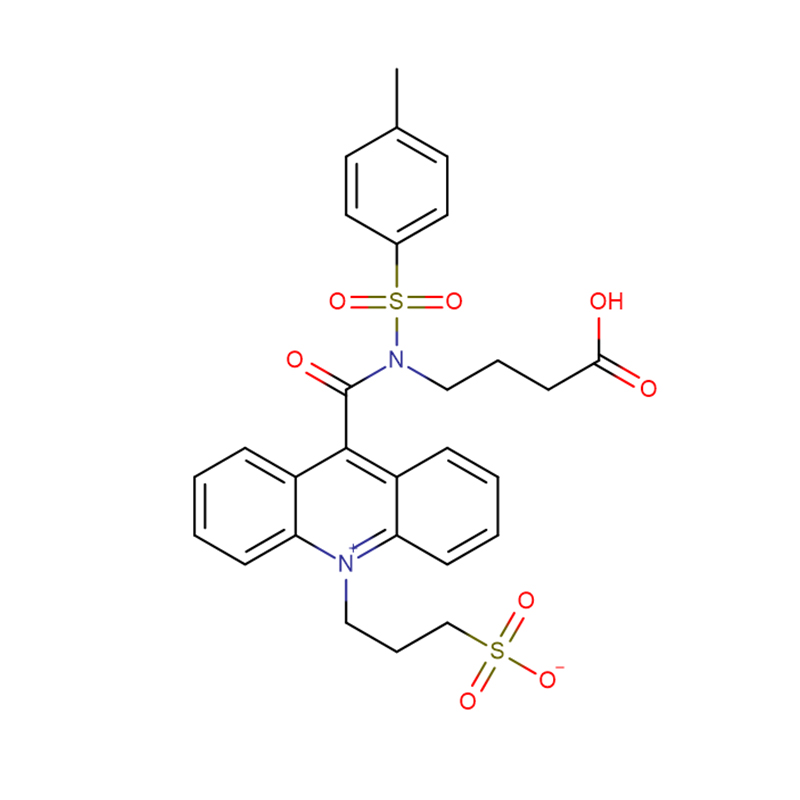
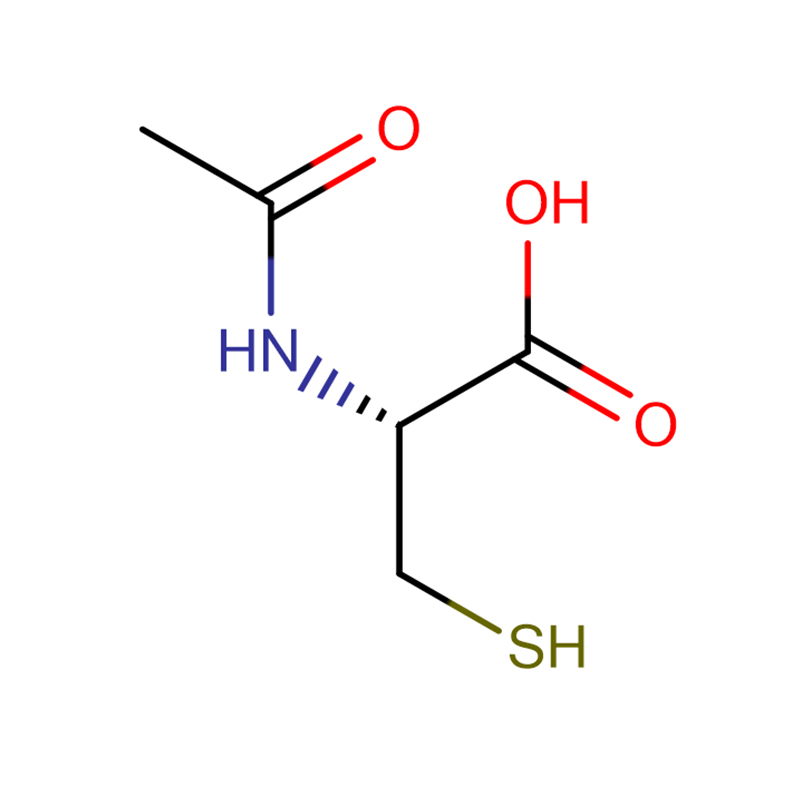
4-Amino-3-hydrazino-1,2,4-triazol-5-thiol Cas:28836-03-5 99% Kuning hingga hijau padat
| Nomor katalog | XD90146 |
| Nama Produk | 4-Amino-3-hidrazino-1,2,4-triazol-5-tiol |
| CAS | 28836-03-5 |
| Formula molekul | C16H13NO3S·NH3 |
| Berat molekul | 316.37 |
| Detail Penyimpanan | Sekelilingnya |
| Kode Tarif Harmonisasi | 2923900090 |
Spesifikasi produk
| Penampilan | Kuning ke hijau padat |
| Assay | ≥ 99% |
| Titik lebur | 237°C(des.)(menyala.) |
| Kelarutan | NaOH: larut1 N |
| Larut dalam air | Larut dalam air, 1N NaOH, dan metanol. |
1. Kami mempelajari efek penghambatan isorhamnetin pada tirosinase jamur dengan kinetika penghambatan dan simulasi komputasi.Isorhamnetin secara reversibel menghambat tirosinase dengan cara tipe campuran pada Ki=0,235±0,013 mM.Pengukuran fluoresensi pengikat intrinsik dan 1-anilinonaphthalene-8-sulfonate (ANS) menunjukkan bahwa isorhamnetin tidak menyebabkan perubahan signifikan dalam struktur tersier tirosinase.Untuk mendapatkan wawasan tentang proses inaktivasi, kinetika dihitung melalui pengukuran interval waktu dan reaksi substrat yang berkelanjutan.Hasilnya menunjukkan bahwa inaktivasi yang diinduksi oleh isorhamnetin merupakan reaksi orde pertama dengan proses biphasic.Untuk mendapatkan wawasan lebih lanjut, kami mensimulasikan docking antara tyrosinase dan isorhamnetin.Simulasi berhasil (energi pengikat untuk Dock6.3: -32,58 kkal/mol, untuk AutoDock4.2: -5,66 kkal/mol, dan untuk Fred2.2: -48,86 kkal/mol), menunjukkan bahwa isorhamnetin berinteraksi dengan beberapa residu, seperti sebagai HIS244 dan MET280.Strategi memprediksi interaksi tirosinase ini dalam kombinasi dengan kinetika berdasarkan senyawa flavanon mungkin berguna dalam skrining potensi penghambat tirosinase alami.
2.Asam membuka jalur conalbumin (CA), glikoprotein monomer dari putih telur ayam, telah diselidiki menggunakan spektroskopi CD jauh dan dekat-UV, emisi fluoresensi intrinsik, probe fluoresensi ekstrinsik 1-anilino-8-napthalene sulfonate (ANS) dan hamburan cahaya dinamis (DLS).Kami mengamati perubahan yang bergantung pada pH dalam struktur CA sekunder dan tersier.Ini memiliki struktur sekunder α-heliks asli pada pH 4,0 tetapi kehilangan struktur pada pH 3,0.CA ada secara eksklusif sebagai keadaan globula pra-cair dan globula cair dalam larutan masing-masing pada pH 4,0 dan pH 3,0.Pengaruh pH pada konformasi dan termostabilitas CA menunjukkan ketahanan panasnya pada pH netral.Hasil DLS menunjukkan bahwa keadaan MG ada sebagai bentuk kompak dalam larutan berair dengan jari-jari hidrodinamik 4,7 nm.Pendinginan fluoresensi triptofan oleh akrilamida lebih lanjut mengkonfirmasi akumulasi keadaan antara, sebagian tidak terlipat, di antara keadaan asli dan tidak terlipat.


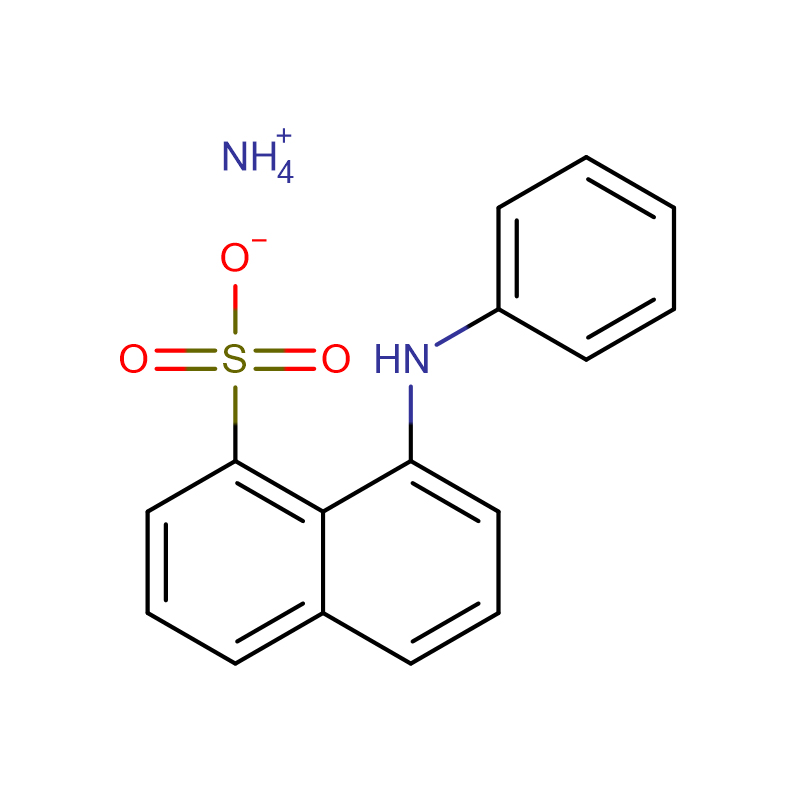


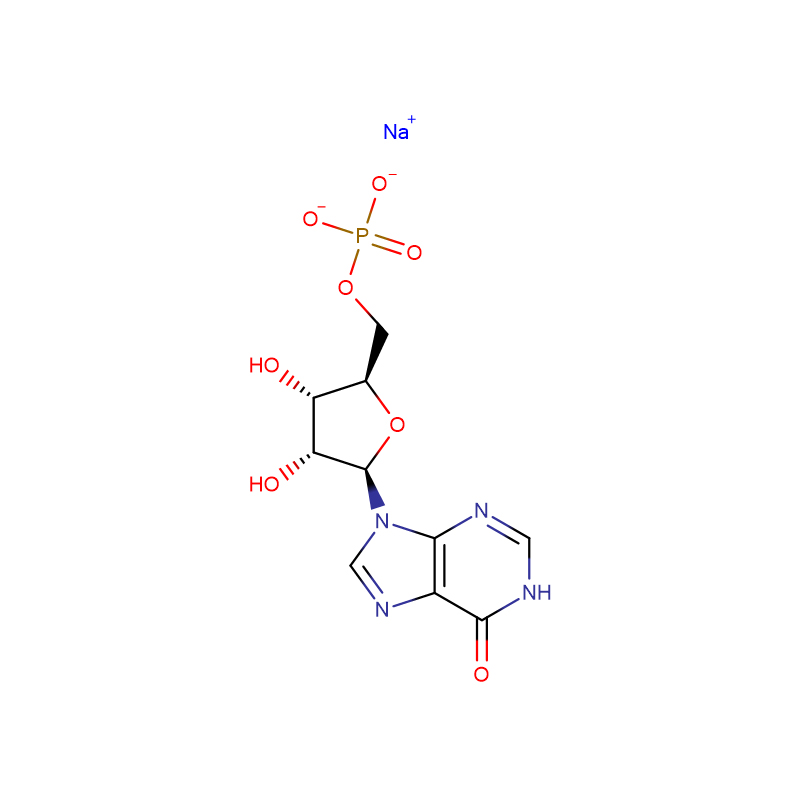
![N-[[bis[4-(dimethylamino)phenyl]amino]carbonyl] glycine sodium salt Bubuk kristal putih sampai abu-abu hijau](http://cdn.globalso.com/xdbiochems/115871-19-7.jpg)